
局部癫痫发作(partial or local epilepsy,PE)是最为常见的癫痫临床类型,发生率占到了约60%。一般认为,PE的主要病因主要是遗传因子,但主要的PE单基因还不明确,目前已鉴定的几个基因,包括例如KCNT1和DEPDC5,仅能解释一小部分PE患者的病因。近日,由国内著名神经病学家廖卫平教授领导的中国癫痫基因1.0计划(the China Epilepsy Gene 1.0 Project)鉴定了PE的一个新致病基因——CELSR1。
该研究由广州医科大学第二附属医院神经科学研究所/第一附属医院儿科、教育部广东省神经发育与信号通路疾病重点实验室、郑州大学第一附属医院儿科、南方医科大学附属佛山妇幼保健院、西安第四军医大学西京医院、汕头潮南民生医院和兰州大学第二医院等多家单位共同完成,并在知名期刊American Journal of Medical Genetics Part B-Neuropsychiatric Genetics发表了这一发现:“CELSR1 variants are associated with partial epilepsy of childhood”。
CELSR1,是一种主要在人类胚胎早期神经干细胞表达的基因,其编码的蛋白属于钙粘蛋白超家族的成员,参与平面细胞极性(PCP)。在高等脊椎动物中,PCP信号在神经管关闭中起重要作用。此前,对CELSR1相关疾病的认知仅有常染色体显性遗传性淋巴畸形。
研究者通过356个PE案例的多中心队列研究,在6个无亲属关系的家系中(其中智因东方提供了部分重要案例线索)鉴定了CELSR1突变与PE临床诊断的因果关联性,从而提出CELSR1是潜在的PE致病基因。有趣的是,在6个案例中,2个是新发的CELSR1杂合性变异致病,4个是复合杂合性变异,这表明CELSR1导致的PE具有常染色体显性或隐性遗传的基因型-表型关联的异质性特征。这一有趣现象也提示出CELSR1更多案例的发现和致病机制研究还有待于更深入的探索。
该研究采用核心家系(父母+子女)全外显子组测序的方法,在排除所有已知的致病基因后,研究者对每个家系,逐步地筛选候选致病变异:1)筛选出SNP数据库中MAF< 0.5%的变异;2)利用生信工具对这些变异的致病性进行评估;3)利用已知的5个遗传病生信分析模型进行致病性变异的进一步筛选:a. 癫痫基因模型、b.新发(de novo)突变显性模型、c.常染色体隐性遗传病模型、d. X染色体连锁模型和e.共分离分析模型。通过以上的分析步骤,研究者筛选出356个家系得到的候选基因,最后发现在6个家系中均存在CELSR1变异。
图1和表1展示了10个CELSR1变异、遗传方式和临床表型特征(诊断)。患者原诊断分类中,6例中有3例被诊断为儿童良性癫痫伴中央颞区棘波,BECTS。此外,6例中半数具有轻度的智力障碍(intellectual disability,ID),提示CELSR1突变与广谱的PE疾病相关。这也反映出,CELSR1-PE在以往的诊断中可能被大大地低估。

▲ 图1 家系图及一代测序
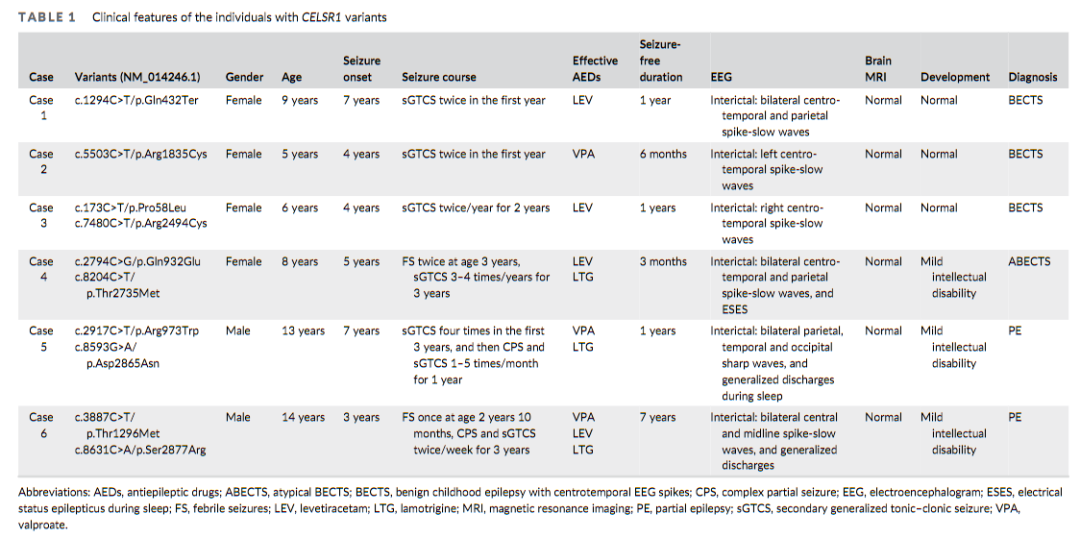
▲ 表1 6个家系患者临床特征
5名患者(案例1-5)EEG表现,主要特征包括中央颞区棘-慢波,其中患者4和5在睡眠期有广泛的持续性棘-慢波,其中患者4呈典型的睡眠中癫痫性电持续状态(electrical status epilepticus during sleep,ESES),这提示与认知受损相关的临床表现(图2)。
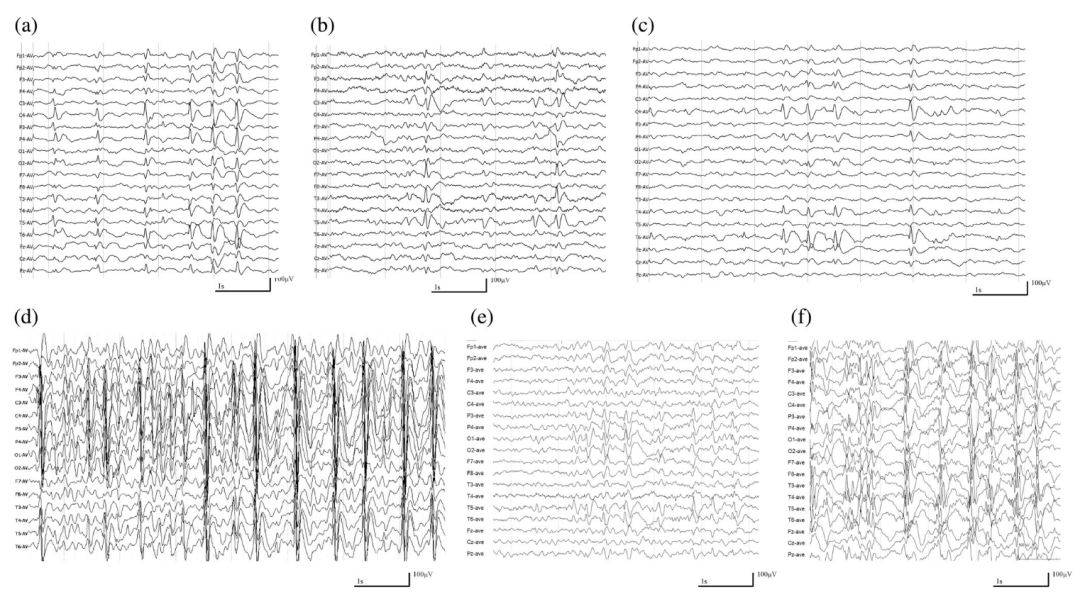
▲ 图2 患者脑电图
研究者通过分子建模发现,所鉴定的10个CELSR1变异都将导致功能性缺失(包括1个无义突变p.Gln432Ter)。有趣的是,9个错义突变均位于细胞内或外信号肽链上,但分布于不同的功能结构域(图3)。9个错义突变在人群数据库中均有分布,表明在以往的一些癫痫的基因诊断中,可能存在对CELSR1和癫痫关联性未知而漏诊现象。
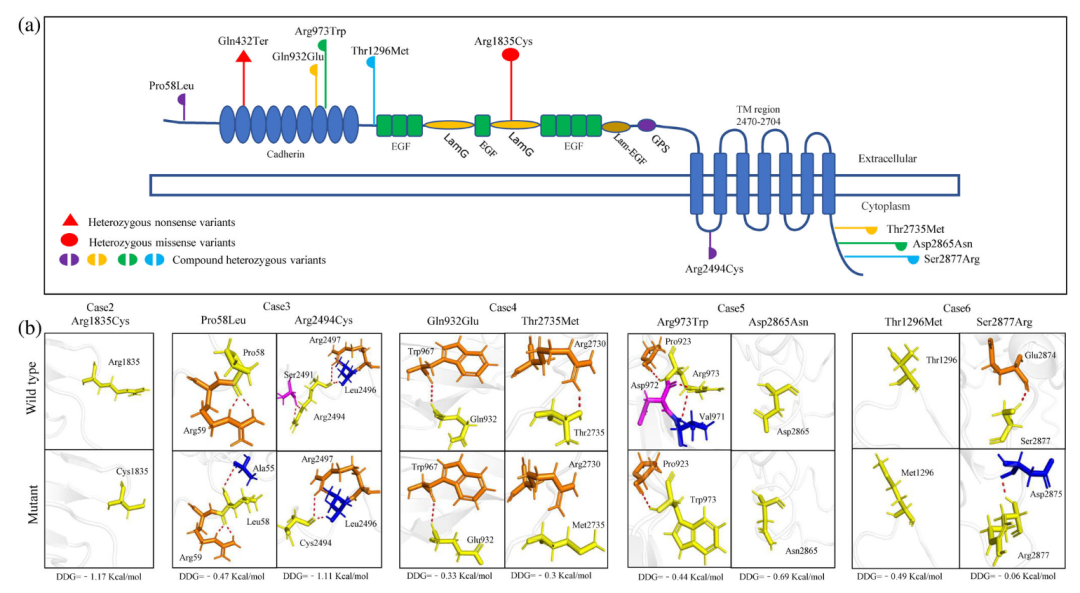
▲ 图3 突变所在结构域及蛋白结构预测图
该研究通过对PE阴性案例的深度剖析,对未知的癫痫基因从基因和变异两个层面进行致评估,结合大量病例,明确了CELSR1是PE的新致病基因,扩展了CELSR1基因的表型谱。
CELSR1基因与癫痫/PE诊断的关联新发现,不仅开拓了对儿童部分性癫痫的病因学新认识,也在提醒着拥有全外显子组数据的临床医师,适时进行阴性结果的回顾性分析,可能会提高既往案例的诊断率;同时,较常见癫痫类型潜在的遗传因子很可能被低估,而借助多中心队列数据聚类分析是探究其病因的有效方式,这种模式或成为未来遗传学研究/新基因探索的趋势。


